25. Februar 20268 min
Medizinisch geprüft: 25.2.2026 • Quellen verifiziert: 25.2.2026
Retatrutide: Ergebnisse der Phase-2-Studien
Zusammenfassung der Phase-2-Studien zu Retatrutide mit Gewichtsverlusten bis zu 24,2 % nach 48 Wochen, Verbesserungen der Blutzuckerkontrolle bei Typ-2-Diabetes und kardiovaskulären Markern.
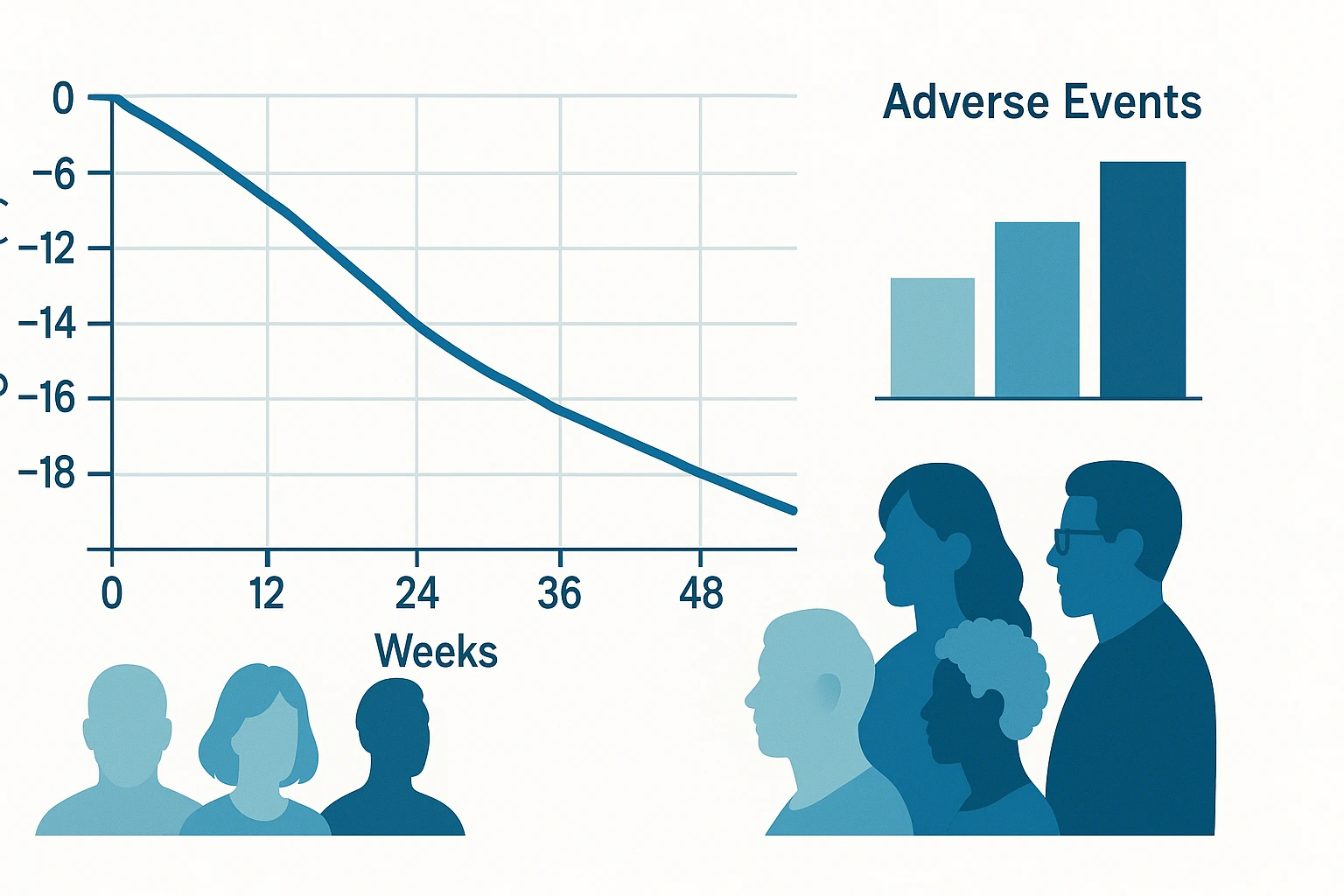
Retatrutide Phase-2-Ergebnisse zeigten einen Gewichtsverlust von bis zu 24,2 % nach 48 Wochen bei der 12-mg-Dosis [1]. Die Studien wiesen auch Verbesserungen der Blutzuckerkontrolle bei Patienten mit Typ-2-Diabetes (T2D) und günstigere Marker für die Herzgesundheit nach [1][3]. Diese Ergebnisse aus Studien von Eli Lilly bilden die Grundlage für Phase-3-Studien, wobei Sicherheitsaspekte wie gastrointestinale Nebenwirkungen zu beobachten sind [1]. Zu Details zur aktuellen Retatrutide-Zulassung durch die EMA siehe unseren Leitfaden.
Einführung in die Retatrutide Phase-2-Ergebnisse
Phase-2-Studien haben dieses neue Medikament bei Adipositas und assoziierten Erkrankungen untersucht. Die Ergebnisse wurden in renommierten medizinischen Fachzeitschriften veröffentlicht und beleuchten sein Potenzial [1].
Wichtige Ergebnisse der Studien
- Höchste Dosis (12 mg): 24,2 % durchschnittlicher Gewichtsverlust nach 48 Wochen, ohne Anzeichen eines Plateaus [1].
- Bei 8 mg oder 12 mg verloren fast alle Teilnehmer (100 %) mindestens 5 % Körpergewicht; 93 % verloren 10 % oder mehr [1].
- Bei T2D-Patienten verbesserte sich die glykämische Kontrolle deutlich mit HbA1c-Reduktionen von 1,3–2,0 % [3].
Diese Studienergebnisse tragen zur Weiterentwicklung von Adipositastherapien bei.
Bedeutung der Ergebnisse für die Behandlung von Adipositas und T2D
Adipositas betrifft Millionen Menschen und erhöht das Risiko für Diabetes, Herzkrankheiten und weitere Erkrankungen. Die Phase-2-Ergebnisse zeigen höhere Gewichtsverluste im Vergleich zu Medikamenten wie Semaglutid oder Tirzepatid in frühen Studien [1].
Bei T2D erreichten bis zu 82 % der Patienten einen HbA1c-Wert unter 6,5 %, was zu weniger Komplikationen führen kann [3]. Insgesamt deuten die Ergebnisse darauf hin, dass Retatrutide Lücken in bestehenden Therapien schließen könnte.
Was ist Retatrutide?
Retatrutide, auch bekannt als LY3437943, ist ein experimentelles Medikament von Eli Lilly. Es wird bei Adipositas, Übergewicht, T2D und Leberfettansammlungen wie NAFLD eingesetzt [1][2].
Wirkmechanismus: Triple-Agonist (GLP-1, GIP, Glukagon)
Im Gegensatz zu Einzel- oder Dual-Agonisten wie Ozempic oder Mounjaro aktiviert Retatrutide drei Schlüsselrezeptoren [1]:
- GLP-1: Reduziert den Appetit und verlangsamt die Verdauung.
- GIP: Fördert die Insulinfreisetzung und unterstützt den Fettstoffwechsel.
- Glukagon: Erhöht den Energieverbrauch und die Fettverbrennung.
Dieser Triple-Wirkmechanismus erklärt die Phase-2-Ergebnisse bei Gewichtsverlust und Metabolismus.
Entwickler: Eli Lilly und Studienübersicht (NCT04881760)
Eli Lilly hat Retatrutide für wöchentliche Injektionen entwickelt. Die Haupt-Phase-2-Studie NCT04881760 umfasste 338 Erwachsene mit Adipositas oder Übergewicht (zunächst ohne T2D) [2].
Subgruppen untersuchten Effekte bei T2D und NAFLD [1][3]. Die Ergebnisse unterstützen den Übergang zu größeren Phase-3-Studien.
Design der Phase-2-Studien und getestete Dosen
Die Studien waren randomisiert, doppelblind und placebokontrolliert, um zuverlässige Daten zu erzeugen [2]. Sie dauerten bis zu 48 Wochen zur Überprüfung langfristiger Effekte [1].
Studienpopulation: Adipositas, Übergewicht, T2D- und NAFLD-Subgruppen
- Hauptgruppe: Erwachsene mit BMI ≥30 (Adipositas) oder ≥27 (Übergewicht) mit Komorbiditäten wie Bluthochdruck [2].
- Subgruppen: Patienten mit T2D oder NAFLD [1][3].
- Gesamt: Ca. 338 in der Adipositas-Studie; weitere in verwandten Studien [2].
Diese diverse Population spiegelt reale Patienten wider.
Dosierungsplan: 1 mg, 4 mg, 8 mg, 12 mg mit schrittweiser Steigerung
Wöchentliche subkutane Injektionen mit langsamer Steigerung zur Minimierung von Nebenwirkungen [1][2]:
| Dosis | Steigerungsstart | Erhaltungsdosis |
|---|---|---|
| 1 mg | Niedrig, konstant | 1 mg wöchentlich |
| 4 mg | Ab 2 mg | 4 mg wöchentlich |
| 8 mg | Ab 2–4 mg | 8 mg wöchentlich |
| 12 mg | Ab 2 mg | 12 mg wöchentlich |
Placebogruppe erhielt Scheininjektionen [2].
Endpunkte: 24 Wochen (primär) und 48 Wochen (sekundär)
- Primär: Prozentuale Gewichtsveränderung nach 24 Wochen [2].
- Sekundär: Gewicht nach 48 Wochen, HbA1c, Lipide, Sicherheit [1].
- Responder: Kategorien wie ≥15 % Verlust [1].
Wirksamkeit von Retatrutide in Phase 2: Gewichtsverlust-Ergebnisse
Die Phase-2-Ergebnisse zeigten eine dosisabhängige und anhaltende Gewichtsreduktion. Höhere Dosen übertrafen Placebo deutlich [1].
Gewichtsreduktion nach 24 Wochen je Dosis (LS-Mittel % Veränderung)
| Dosis | % Veränderung | Placebo-korrigiert |
|---|---|---|
| 1 mg | -7,2 % | -5,6 % |
| 4 mg | -12,9 % | -11,3 % |
| 8 mg | -17,3 % | -15,7 % |
| 12 mg | -17,5 % | -16,0 % |
| Placebo | -1,6 % | - |
Absoluter Verlust bei 12 mg: 18,7 kg [1][2].
Gewichtsverlust nach 48 Wochen: Bis zu 24,2 % bei 12 mg (kein Plateau)
Das Gewicht nahm bis 48 Wochen weiter ab [1]:
| Dosis | % Veränderung | Placebo-korrigiert | Absoluter Verlust (12 mg Beispiel) |
|---|---|---|---|
| 1 mg | -8,7 % | -6,6 % | - |
| 4 mg | -17,1 % | -15,0 % | - |
| 8 mg | -22,8 % | -20,7 % | - |
| 12 mg | -24,2 % | -22,1 % | 26,3 kg |
| Placebo | -2,1 % | - | - |
Kein Plateau deutet auf anhaltende Effekte hin [1].
Gewichtsverlust-Meilensteine: ≥5 %, ≥10 %, ≥15 % Responder
Nach 48 Wochen (12 mg Dosis) [1]:
- ≥5 %: 100 % der Teilnehmer.
- ≥10 %: 93 %.
- ≥15 %: 83 %.
Schon 4 mg erreichte 92 %/75 %/60 %. Hohe Responder-Raten fielen auf.
Absoluter Gewichtsverlust (kg) und Placebo-Vergleich
Eine Person mit 90,7 kg Körpergewicht könnte bei 12 mg nach 48 Wochen ca. 21,8 kg verlieren. Placebo verlor im Mittel nur 1,8 kg. Überlegen gegenüber vielen zugelassenen Medikamenten [1].
Glykämische Kontrolle und T2D-Ergebnisse in Phase 2
In T2D-Subgruppen verbesserten sich die Blutzuckerwerte über den Gewichtsverlust hinaus [1][3].
HbA1c-Reduktionen: 1,3–2,0 % je Dosis
Über 24–36 Wochen [3]:
- 4 mg: -1,3 %.
- 8–12 mg: Bis zu -2,0 %.
Bedeutende Reduktionen bei unkontrolliertem T2D.
Erreichungsraten: Bis zu 82 % <6,5 % HbA1c, 31 % <5,7 %
- <6,5 % (Ziel): 82 % bei höheren Dosen [1].
- <5,7 % (normal): 31 % [1].
Nüchternblutzucker sank ebenfalls stark.
Vergleich zu Dulaglutid
Retatrutide übertraf Dulaglutid 1,5 mg (ein GLP-1-Medikament) bei HbA1c und Gewicht [1]. Doppelter Nutzen für T2D-Patienten.
Kardiovaskuläre und metabolische Verbesserungen aus Retatrutide Phase 2
Die Phase-2-Ergebnisse zeigten Verbesserungen kardiovaskulärer und metabolischer Marker über den Gewichtsverlust hinaus [1].
Taillenumfang, Blutdruck, Lipide (Triglyzeride, Non-HDL)
- Taillenumfang: Reduktion um 18–25 cm bei höheren Dosen [1].
- Blutdruck: Systolische Senkung um 5–8 mmHg [1].
- Lipide: Triglyzeride um 25–30 % gesenkt; Non-HDL-Cholesterin verbessert [1].
Diese Veränderungen reduzieren kardiovaskuläre Risiken.
Vorteile in NAFLD-Subgruppe und keine Hepatotoxizität
Bei NAFLD-Patienten entsprach der Gewichtsverlust dem der anderen; Leberenzyme blieben stabil oder verbesserten sich. Keine Lebersicherheitsprobleme nach 48 Wochen [1].
Sicherheitsprofil und Nebenwirkungen in den Retatrutide Phase-2-Ergebnissen
Die Phase-2-Ergebnisse zeigten ein Sicherheitsprofil vergleichbar mit zugelassenen GLP-1-Medikamenten. Die meisten Ereignisse waren beherrschbar [1].
Häufigkeit unerwünschter Ereignisse: 73–94 %, meist milde bis moderate GI
73–94 % berichteten Ereignisse, dosisabhängig steigend. Schwere Ereignisse selten [1].
Häufige Nebenwirkungen: Übelkeit, Erbrechen, Durchfall während Steigerung
- Übelkeit: 40–60 %, frühzeitiger Peak [1].
- Erbrechen/Durchfall: 20–40 % [1].
- Überwiegend in der Aufdosierphase; nahmen mit der Zeit ab.
Herzfrequenzveränderungen: Dosisabhängig, Peak nach 24 Wochen
Erhöhungen um 5–10 bpm bei höheren Dosen, Maximum in Woche 24, dann Rückgang. Engmaschige Überwachung [1].
Abbrüche (6–16 %) und schwere Ereignisse (0–6 %)
- Abbrüche: 6 % (1 mg) bis 16 % (12 mg) vs. 0 % Placebo [1].
- Schwere Ereignisse: 0–6 % vs. 4 % Placebo [1].
Keine Todesfälle oder große Bedenken.
Minderungsstrategien und Vergleich zu GLP-1-Agonisten
Langsame Steigerung und niedrige Starts reduzierten GI-Probleme. Sicherheit vergleichbar mit Semaglutid/Tirzepatid [1]. Zum Rechtsstatus von Retatrutide in der EU nach Phase 2 gilt es derzeit als Forschungsmittel.
Veröffentlichung und Studienstatus nach Phase 2
Die Ergebnisse erhielten Glaubwürdigkeit durch Peer-Review [1].
NEJM-Veröffentlichung (PMID: 37366315)
Detailliert in NEJM (2023) [1]. Bestätigt Wirksamkeits- und Sicherheitsdaten.
Phase-3-TRIUMPH-Programm: Laufende Bestätigungsstudien
TRIUMPH Phase 3 testet größere Gruppen mit aktiven Komparatoren [4]. Retatrutide-Zulassungs-Tracker für EMA, BfArM und TGA-Updates für aktuelle Fortschritte.
Regulatorischer Status und Weg zur EMA-Zulassung
Phase-2-Erfolge haben Retatrutide vorangebracht, Zulassung erfordert jedoch Phase-3-Daten [1][4].
Aktueller regulatorischer und EMA-Status nach Phase 2
Nicht EMA-zugelassen; rein investigativ. Verfügbarkeit über Studien/Mitleid? Siehe Ist Retatrutide derzeit in der EU legal?.
Bedeutung der Phase-2-Ergebnisse für zukünftige Zulassung
Starke Wirksamkeit und Sicherheit unterstützen schnelle Weiterentwicklung. Phase 3 zur Bestätigung; Zulassung möglich ab 2026–2027 bei Erfolg [1][4]. Siehe Ist Retatrutide EMA-zugelassen? zur Rolle von Phase 2 in Zeitplänen.
Fazit: Zukunft von Retatrutide basierend auf Phase-2-Daten
Die Retatrutide Phase-2-Ergebnisse zeigen bis zu 24 % Gewichtsverlust, T2D-Kontrolle und kardiovaskuläre Vorteile bei akzeptabler Verträglichkeit [1].
Zusammenfassung von Wirksamkeit, Sicherheit und nächsten Schritten
- Wirksamkeit: Hoher Gewichtsverlust ohne Plateau [1].
- Sicherheit: GI-dominiert, vergleichbar mit anderen; Herzfrequenz überwachen [1].
- Nächste Schritte: Phase-3-TRIUMPH-Ergebnisse [4]. Retatrutide-Zulassungs-Tracker für aktuelle EMA/BfArM-Fortschritte.
Potenzielle Auswirkungen auf Adipositastherapien
Die Phase-2-Ergebnisse positionieren Retatrutide im Vergleich zu aktuellen Therapien. Semaglutid erzielt typischerweise 15–17 % Gewichtsverlust, Tirzepatid 20–22 % – Retatrutide erreichte 24,2 % mit anhaltendem Fortschritt und ohne Plateau [1]. Dies könnte mehr Patienten klinisch relevante Ziele wie 15–20 % Verlust erreichen lassen und Risiken für T2D, Herzkrankheiten und NAFLD mindern.
Bei Bestätigung in Phase 3 könnte Retatrutide Standards neu definieren als potente wöchentliche Option neben Lebensstilmaßnahmen. Wettbewerb könnte Kosten senken und Zugang verbessern. Patienten und Ärzte sollten Entwicklungen beobachten – konsultieren Sie einen Facharzt für evidenzbasierte Therapien bei Adipositas. Siehe Tirzepatid vs. Retatrutide für Vergleiche.
Referenzen
-
Jastreboff AM, Aronne LJ, Ahmad NN, et al. Triple-Hormone-Receptor Agonist Retatrutide for Obesity - A Phase 2 Trial. N Engl J Med. 2023;389(6):514-526. doi:10.1056/NEJMoa2301972. Volltext; PMID: 37366315.
-
ClinicalTrials.gov. NCT04881760: Retatrutide (LY3437943) in Participants Who Have Obesity or Overweight With Weight-Related Comorbidities Without Diabetes. U.S. National Library of Medicine. Studienprotokoll.
-
ClinicalTrials.gov. NCT04867785: Retatrutide (LY3437943) in Participants With Type 2 Diabetes (OBESE). U.S. National Library of Medicine. Studienprotokoll.
-
ClinicalTrials.gov. NCT05929066: A Study of Retatrutide (LY3437943) in Participants Who Have Obesity or Overweight With Weight-Related Comorbidities Without Diabetes (TRIUMPH-1). U.S. National Library of Medicine. Phase-3-Studienprotokoll.
Verwandte Artikel
- /articles/is-retatrutide-fda-approved – EMA-Status-Update.
- /articles/retatrutide-approval-tracker-fda-ema-tga – Globale Tracker.
- /articles/is-retatrutide-legal-in-us – EU-Rechtslage.
- /articles/semaglutide-vs-retatrutide – Vergleiche.
- /articles/tirzepatide-vs-retatrutide – Dual- vs. Triple-Agonisten.
Medizinische Beratung zu Inkretin-basierten Therapien
Für die Evaluation zugelassener Adipositas-Therapien konsultieren Sie in der EU lizensierte Telemedizin-Anbieter oder Ihren behandelnden Arzt.